刘文娟,肖 莹,买占海,张晓松,周 轲,姚万玲,纪 鹏,华永丽,袁子文,魏彦明
(甘肃农业大学动物医学院,甘肃兰州 730070)
为维护我国动物源性食品安全和公共卫生安全,中华人民共和国农业农村部公告第194号明确规定,自2020年7月1日起,饲料生产企业停止生产含有促生长类药物饲料添加剂(中药类除外)的商品饲料。在“饲料端禁抗、养殖端限抗”背景下,畜禽高效健康养殖的新型替抗饲料添加剂产品需求日益迫切。中药作为新型替抗饲料添加剂产品的重要来源之一,应用前景广阔。
黄芪和当归均为甘肃省道地药材。黄芪为豆科植物荚膜黄芪或蒙古黄芪的根,性微温,味甘;
入肺、脾经,主要含有多糖、黄酮类、皂苷类及氨基酸、微量元素等有效成分[1]。当归为伞形科植物当归的干燥根,性温,味甘、辛;
归肝、心、脾经[2],主要成分为多糖、有机酸和挥发油等[3]。自古以来有“十方九归”的说法[4],可见其应用广泛。查阅古方及大量文献发现,符合“气血同补”理念的黄芪当归配伍在临床上应用广泛,常用比例包括1∶1、3∶1、1∶5、3∶2、2∶1及5∶1等[5]。有学者发现,黄芪-当归(1∶1)配伍对提高小鼠免疫力效果较显著[6];
且促进造血作用较强[7-9]。研究发现黄芪当归按1∶1配伍时,提取物中主要活性成分阿魏酸、黄芪甲苷、芒柄花素、毛蕊异黄酮、毛蕊异黄酮苷等成分的溶出量显著增加,在小肠中的吸收量也呈增加趋势[10]。但截至目前关于黄芪-当归(1∶1)水提物制备工艺优化的报道甚少。因此,本研究通过测定黄芪-当归(1∶1)水提物中阿魏酸(Y1)、毛蕊异黄酮(Y2)、粗多糖(Y3)及干浸膏(Y4)含量占比,以此进行综合评分,在单因素试验基础上进行L9(34)正交试验,优选黄芪-当归(1∶1)水提工艺,旨在为黄芪当归提取物作为饲料添加剂进行工业化生产及质量标准控制提供理论依据。
1.1 材料
1.1.1 药材 中药材黄芪(批号:HZ20210105)、当归(批号:HZ20210120)均购自兰州黄河药材市场,经甘肃农业大学动物医学院中兽医学教研室鉴定分别为豆科植物黄芪、伞形科植物当归的干燥根。
1.1.2 试剂 阿魏酸标准品(批号:F103702 ),阿拉丁公司产品;
毛蕊异黄酮标准品(批号:yz170221),南京源植生物技术公司产品;
D-无水葡萄糖(批号:50-99-7),上海凛恩科技发展有限公司产品;
乙腈、甲醇为色谱纯;
其他试剂为分析纯。
1.1.3 主要仪器 JA2003电子天平,上海舜宇恒平科学仪器有限公司产品;
Aglient1260高效液相色谱仪,安捷伦科技有限公司产品;
RE-6000旋转蒸发仪,上海亚荣生化仪器厂产品;
FD-1A-5D型冷冻干燥机,北京博医康实验仪器有限公司产品;
Spectra Max Plus384酶标仪,美谷分子仪器有限公司产品。
1.2 方法
1.2.1 水提工艺 将黄芪、当归饮片粉碎后过60目筛,精确称量黄芪、当归药粉各5 g混合均匀,据设定的时间、料液比、温度及提取次数进行提取,提取液经4 000 r/min离心10 min,收集上清液,在60 ℃下旋转蒸发浓缩、并经冷冻干燥后备用。
1.2.2 阿魏酸与毛蕊异黄酮的含量检测
1.2.2.1 色谱条件 色谱柱:Agilent ZORBAX SB-C18柱 (250 mm×4.6 mm, 5 μm) ;
流动相:乙腈(A)-1 mL/L磷酸水溶液(B);
洗脱梯度:10 min~16 min 20%A;
16 min~25 min 20%~32%A;
25 min~34 min 32%~34%A。柱温35 ℃;
流速0.8 mL/min;
检测波长280 nm;
进样量20 μL。
1.2.2.2 对照品溶液的制备 精密称取阿魏酸和毛蕊异黄酮对照品适量,加入甲醇溶解并定容,制成每1 mL含阿魏酸0.1 mg、毛蕊异黄酮0.035 mg的混合对照品母液。
1.2.2.3 供试品溶液的制备 精密称取“1.2.1”项下提取制备的提取物300 mg,加甲醇溶解,3 500 r/min离心10 min,将上清液移至10 mL容量瓶中加甲醇定容至刻度线,0.45 μm微孔滤膜过滤取其续滤液。
1.2.2.4 样品含量测定 按照“1.2.2.3”项下方法制备供试品溶液,按照“1.2.2.1”项下色谱条件进样分析,记录阿魏酸与毛蕊异黄酮的保留时间和峰面积,采用外标法分别计算其含量。
1.2.3 粗多糖的测定
1.2.3.1 对照品溶液的制备 精密称取D-无水葡萄糖粉末适量,溶解并定容至100 mL容量瓶中,制成每1 mL含0.25 mg的D-无水葡萄糖标准溶液,作为对照品溶液,4 ℃保存备用。
1.2.3.2 供试品溶液的制备 精密称取“1.2.1”项下提取制备的粉末适量,溶解并定容后制成每1 mL含2 mg样品的供试品溶液,4 ℃保存备用。
1.2.3.3 样品含量测定 在“1.2.3.2”项下制备的供试品溶液中,分别加入1 mL 50 mg/mL的苯酚溶液,迅速在试管中加入5 mL浓硫酸,置漩涡混匀器摇匀后于40 ℃水浴保温加热15 min,取出后冷水冷却10 min,然后精密吸取200 μL反应液于96孔板中,用酶标仪490 nm处测定OD值并记录。
1.2.4 干浸膏得率的测定 干浸膏得率(Y4)=干浸膏质量(m)/原药材质量(M)×100%。
1.2.5 综合加权评分计算 采用综合加权评分法评估黄芪-当归(1∶1)提取工艺,根据其药理作用及结合生产实践方面的利用价值[1,5,11-14],将阿魏酸占比(Y1)、毛蕊异黄酮占比(Y2)、多糖占比(Y3)及干浸膏得率(Y4)的权重系数设为0.2、0.2、0.3、0.3。综合评分=(Y1/Y1max)×100×0.2+(Y2/Y2max)×100×0.2+(Y3/Y3max)×100×0.3+(Y4/Y4max)×100×0.3。式中Y1max、Y2max、Y3max、Y4max分别指代提取物阿魏酸最大占比、毛蕊异黄酮最大占比、粗多糖最大占比、干浸膏最大得率。
1.2.6 单因素试验 精密称取黄芪当归药粉各5 g,水浴加热提取1次,分别考察提取温度为60、70、80、90、100 ℃,提取时间为30、40、50、60、70 min,料液比为1∶5、1∶10、1∶15、1∶20、1∶25对提取工艺的影响。每组试验重复3次。各提取物分别按“1.2.2.4”、“1.2.3.3”“1.2.4”项下方法测定,计算阿魏酸、毛蕊异黄酮、多糖含量占比和干浸膏得率,并按照“1.2.5”项下方法进行综合评分计算。
1.2.7 正交试验设计 以单因素试验初步筛选结果为基础,分别以提取温度、提取时间、料液比为因素,再加入提取次数因素(1次、2次、3次),进行4因素3水平的L9(34)正交试验,优选黄芪当归水提物制备工艺(表1)。
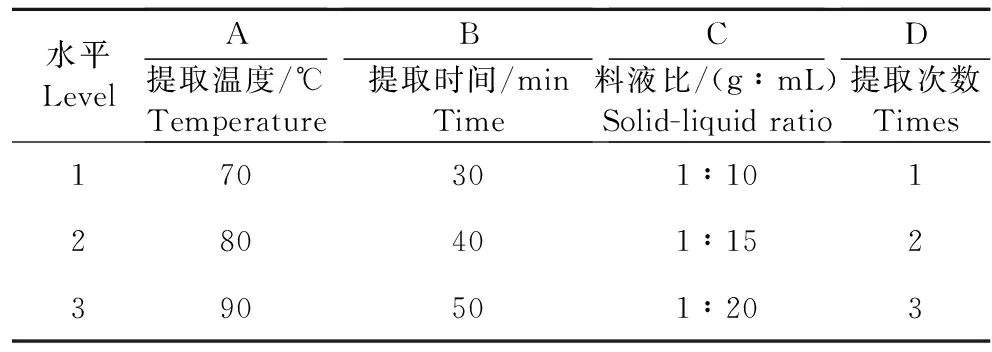
表1 正交试验水平
2.1 阿魏酸与毛蕊异黄酮的含量检测
2.1.1 线性关系考察 将混合对照品母液记为1号瓶,再取4个10 mL容量瓶依次标号为2、3、4、5,从1号瓶中取5 mL混合对照品移至2号瓶中,加甲醇定容至10 mL,摇匀,依次稀释到3、4、5号瓶中,稀释倍数分别为2、4、8、16。混和对照品及黄芪-当归(1∶1)水提物供试品的高效液相色谱图见图1。分别从1~5号瓶取20 μL混合对照品溶液,按照“1.2.2.1”项下色谱条件测定峰面积,以色谱峰面积(y)为纵坐标,浓度(x,mg/mL)为横坐标,绘制标准曲线,得回归方程:阿魏酸y=79 587x-202.18(R2=0.999 1),毛蕊异黄酮y=79 922x-33.220 8 (R2=0.999 8)。结果显示,阿魏酸、毛蕊异黄酮检测范围分别在0.006 25 mg/mL~0.1 mg/mL,0.002 187 5 mg/mL~0.035 mg/mL范围内与峰面积呈良好的线性关系。
2.1.2 精密度试验 精密吸取混合对照品溶液20 μL,注入液相色谱仪,连续进样6次,测定并计算得到阿魏酸和毛蕊异黄酮峰面积的RSD值分别为1.01%、1.77%,表明仪器精密度良好。

A.混合对照品;
B.黄芪-当归药对供试品;
C.缺少黄芪的阴性对照;
D.缺少当归的阴性对照;1号和2号峰分别阿魏酸、毛蕊异黄酮
2.1.3 重复性试验 分别精密称取同一条件制备的黄芪当归(1∶1)提取物粉末6份,按“1.2.2.3”项下方法制备供试品溶液,测定并计算得到阿魏酸和毛蕊异黄酮峰面积的RSD值分别为1.06%、2.3%,表明该方法重复性良好。
2.1.4 稳定性试验 取同一黄芪当归提取物粉末适量,按照“1.2.2.3”项下方法制备供试品溶液,室温保存,分别于 0、2、4、6、8、10、24 h 精密吸取20 μL,进样测定,计算得到阿魏酸酸和毛蕊异黄酮峰面积的RSD值分别为2.53%、2.18%,表明供试品溶液在24 h内稳定性良好。
2.1.5 加样回收率 取已知含量提取物粉末6份,分别精密加入混合对照品溶液适量,按“1.2.2.3”项下方法制备供试品溶液,注入液相色谱仪,测定计算得到阿魏酸和毛蕊异黄酮平均加样回收率分别为103.9%、100.19%,RSD分别为1.61%、2.93%,表明该方法准确度良好。
2.2 粗多糖的测定
2.2.1 线性关系考察 用移液管分别移取“1.2.3.1”项下制备的对照品溶液0、0.1、0.2、0.4、0.6、0.8、1.0 mL分别置于不同的试管之中,加蒸馏水至2.0 mL。后续操作同“1.2.3.3”项下方法。以浓度(x,mg/mL)为横坐标,OD值为纵坐标,绘制标准曲线,结果表明在0~0.031 25 mg/mL浓度范围内线性关系良好,求得出回归方程为:y=29.178x-0.015 4,R2=0.999 0。
2.2.2 精密度试验 精确吸取D-无水葡萄糖对照品溶液0.6 mL置试管中,按照标准曲线操作步骤重复测定6次,测定并计算得到RSD值为0.597%,说明仪器精密度良好。
2.2.3 重复性试验 分别精密称取同一条件制备的黄芪-当归(1∶1)提取物粉末6份,按“1.2.3.2”项下方法制备供试品溶液,测定并计算得到RSD值为2.29%,表明该方法重复性良好。
2.2.4 稳定性试验 取完全反应后的供试品,每隔20 min测1次OD值,测定并计算OD值的RSD为1.42%,说明在100 min内样品稳定性良好。
2.2.5 加样回收率试验 取已知多糖含量的供试液6份各50 μL至离心管中,按低、中、高浓度分别加已知浓度的对照品溶液用“1.2.3.3”项下方法处理,测定并计算OD值,结果显示样品平均回收率为 98.78%,RSD为0.88%,说明试验准确度良好。
2.3 单因素试验
结果显示,提取温度在80 ℃时,药物提取的综合评分最高。时间在40 min时,药物提取的综合评分最高。料液比在1∶15时,药物提取的综合评分最高。因此,确定80 ℃为最佳提取温度,40 min为最佳提取时间,1∶15为最佳料液比(图2)。
2.4 正交试验设计
根据各指标权重计算综合评分,用正交设计助手软件进行直观分析(表2)。
根据单因素初筛选试验结果及正交设计助手分析结果,分别确定提取温度、时间、料液比、提取次数4个因素,进行方差分析(表3)。
由表2、3可以看出,提取黄芪当归对最优工艺为A2B2C2D3,即提取温度为80 ℃、提取时间为40 min,料液比为1∶15、提取次数为3次。提取次数对其综合评分影响最大,提取温度对综合评分影响最小。
2.5 优化工艺的验证
依据正交试验数据分析所得出的提取工艺,进行3次重复试验(表4)。综合评分分别为98.721、97.888、98.634,RSD值为0.465%。其结果高于前面试验的综合评分,表明此优化工艺可行。

A.温度;B.时间;C.料液比

表2 正交直观分析

表3 方差分析结果

表4 工艺优化验证试验结果
黄芪是重要补气药物之一,当归是重要补血药物之一,二者配伍作为补气生血的重要药对,临床应用潜力较大,其主要通过增强动物机体免疫、增强骨髓造血等功能来发挥药理作用[7]。二者配伍后的化合物主要包括黄酮类的毛蕊异黄酮、毛蕊异黄酮苷、刺芒柄花素、刺芒柄花素苷,有机酸类的阿魏酸、香草酸,以及多糖类等[15]。毛蕊异黄酮是黄芪主要活性成分之一,具有抗氧化、抗过敏、抗肿瘤、保护脏器、抗黑色素再生成等作用[16]。《中国药典》2020 年版中黄芪虽以毛蕊异黄酮葡萄糖苷作为指示成分[17],但在水提过程中,毛蕊异黄酮葡萄糖苷会因持续加热较长时间而易脱去葡萄糖转变为毛蕊异黄酮。毛蕊异黄酮由于相对分子质量小且具有疏水性,相比与它对应的糖苷,更易被吸收而发挥药效[6],且大多数学者都将其作为黄芪质量控制的标志物之一。阿魏酸是《中国药典》2020年版中当归质量控制的唯一指标性成分,具有抗炎、抗氧化、抗血栓、抗辐射及提高机体免疫力等作用,现已广泛应用于医药、食品、化妆品等领域[18]。多糖作为黄芪、当归的重要天然活性成分,具有抗氧化、增强免疫、保肝等生理功能,在畜禽生产中作为饲料添加物被广泛使用[19-21]。另外,文献报道干浸膏率是影响提取工艺产量优化的重要因素[22]。所以,本研究选取阿魏酸、毛蕊异黄酮、多糖3种代表活性成分结合干浸膏得率为检验指标。并根据其化学和药理特性及在优化工艺过程中的重要性,设置不同的权重系数,即阿魏酸、毛蕊异黄酮、多糖分别为 0.2、0.2、0.3,干浸膏得率为0.3。
中药提取工艺的优化是保障中药功效的重要手段。水提工艺优化设计过程中,发现提取时间、提取次数、料液比等因素对提取物的活性及得率有较大影响。本研究在单因素试验过程中发现,当其他条件固定时,随着时间的增加,提取物中阿魏酸占比呈现增加趋势,干浸膏得率、毛蕊异黄酮及多糖占比先升高后降低;
随着温度的增高,干浸膏得率、提取物中阿魏酸及多糖占比先升高后降低,毛蕊异黄酮占比持续降低;
随着料液比的增加,干浸膏得率先增加后基本保持不变,提取物中阿魏酸、毛蕊异黄酮及多糖占比先升高后降低。单因素试验结果显示所选各指标间变化趋势未达成一致,说明若选用单一活性成分作为考察指标无法客观反映药对制备工艺的优劣性。本研究在单因素试验基础上,结合多指标综合评分法开展正交设计试验。多指标综合评分法可兼顾中药复方多靶点多途径的作用特点,有效避免单一指标评价制备工艺时的片面性,更符合中(兽)医用药的整体观思维[23]。正交设计是目前应用最为广泛且发展成熟的多因素多水平试验设计方法之一[24],其具有高效方便、试验次数少、结果直观易分析等特点[25],被广泛运用于生物医药科学领域来解决多因素多水平问题[26-27],从而达到提高生产效率和优化生产工艺等目的。本研究将以上两种试验方法结合,在较少的试验次数中快速确定黄芪-当归(1∶1)水提物最佳制备工艺为:温度80 ℃、提取时间40 min、料液比1∶15、提取3次。
综上所述,本研究就黄芪-当归(1∶1)水提物制备工艺的影响因素,应用正交试验设计法展开工艺性探讨,通过对黄芪-当归常用且稳定的3种活性成分进行检测及干浸膏得率的计算,结合多指标综合评分法分析在现代科学技术下黄芪当归的发展。结果表明,本法简便、重复性好,提取工艺稳定可行,能有效提高药物药效,避免浪费药材,为其作为畜禽保健型饲料添加剂提供理论依据。但本研究也存在一定的不足之处,仅选取主要指标成分作为评价指标,无法全面准确地反映复方中药的物质作用基础。
猜你喜欢 毛蕊浸膏异黄酮 运用血清药理学初步探讨毛蕊异黄酮苷的血管新生作用世界科学技术-中医药现代化(2021年12期)2021-04-19不同温度、pH、光照条件下毛蕊花苷的降解动力学食品工业科技(2020年21期)2020-11-19青橄榄浸膏的提取及其抗氧化活性研究天然产物研究与开发(2019年1期)2019-03-01LC-MS测定黑豆中异黄酮和花色苷的含量天然产物研究与开发(2018年5期)2018-06-13补肺活血胶囊中毛蕊异黄酮葡萄糖苷、毛蕊异黄酮的测定方法中山大学学报(自然科学版)(中英文)(2017年6期)2017-12-22中药浸膏粉吸湿性的评价方法中成药(2017年5期)2017-06-13HPLC法同时测定天山岩黄芪中4 种异黄酮中成药(2017年6期)2017-06-13反相高效液相色谱法测定暖宫孕子丸浸膏中黄芩苷含量中国药业(2014年21期)2014-05-26温度对3种中药浸膏片包衣工艺参数的影响中国药业(2014年4期)2014-05-09HPLC测定芪卫颗粒中毛蕊异黄酮葡萄糖苷的含量中医研究(2014年4期)2014-03-11