雷少帆,苏 锋,齐敏杰,常林荣
(1.浙江超威创元实业有限公司,浙江湖州 313100;
2.超威集团电源有限公司,浙江湖州 313100)
尖晶石锰酸锂具有成本低、环境友好、电压高等优点,使得锰酸锂-石墨电池成为最有前景的动力电池之一[1-4]。然而其较差的高温循环寿命与自放电率大的问题成为限制其大规模使用的瓶颈[1-9]。关于锰酸锂正极材料的失效机理可归纳为:Mn 元素的溶解、锰酸锂中氧缺陷的增多与高电压区的两相共存结构在高温下稳定性的降低[7-13]。为提高锰酸锂-石墨电池的高温循环寿命,一方面,锰酸锂表面包覆与锰酸锂体相掺杂被广泛研究,用以抑制Mn 元素的溶解与提高锰酸锂晶体的稳定性[1,3,14];
另一方面,锰酸锂电解液配方被优化,以减缓Mn 元素溶解与抑制Mn 在负极表面的沉积,如添加丙烯基-1,3 磺酸内酯与碳酸亚乙烯酯[15-17]。目前,研究多集中于锰酸锂的包覆、体相掺杂与长寿命锰酸锂电解液开发的方向。实际生产中,采用Al2O3包覆锰酸锂、含丙烯基-1,3 磺酸内酯与碳酸亚乙烯酯添加剂的电解液提高锰酸锂-石墨电池的高温循环寿命。因而,有必要揭示锰酸锂-石墨电池容量减少的原因,为开发长寿命锰酸锂-石墨电池提供理论依据。
1.1 实验电池
选用超威创元实业有限公司量产的软包锂离子电池,正极活性物质为锰酸锂(质量分数96%)、导电剂(质量分数2%)、聚偏氟乙烯(质量分数2%),负极活性物质为石墨(质量分数94.9%)、导电剂(质量分数1%)、羧甲基纤维素钠(质量分数1.8%)、丁苯橡胶(质量分数2.3%)。正极涂布单面面密度设计为1.98 mAh/cm2,正极涂布单面面密度设计为2.16 mAh/cm2,额定容量为12 Ah,工作电压为3.0~4.2 V。Al2O3包覆锰酸锂正极材料由焦作伴侣纳米材料工程有限公司提供,电解液由珠海市赛纬电子材料股份有限公司提供。为记录循环过程中正负极片电极电位的变化,在手套箱中将软包电芯正面割开一缺口,塞入金属锂片作为参比电极,即为三电极电池。使用日立RL8400-21 型数据记录仪记录正负极片电极电位(vs.Li/Li+)。实验电池与三电极电池如图1 所示。待电池完成OCV2 检测后,对电池进行分容,选取9 只容量、内阻接近的电池作为实验电池。

图1 电池照片
1.2 充放电测试
采用新威BTS-5V/30A-4023 型号充放电柜与巨孚ECT-100-40-TP-AR 型号恒温箱测试电池高温充放电循环性能,实验温度为45 ℃。电池采用恒流恒压方式充电,充电倍率为0.5C,充电截止电流为0.05C,放电采用恒流方式放电,放电倍率为1.0C。容量保持率由式(1)算出:

式中:C1为电池的初始放电容量;
Ci为电池循环i次的放电容量。
1.3 X 射线衍射测试
采用内标法校准仪器误差,并测量锰酸锂与石墨的面间距。当电池循环1、50、100、150、200、250、300、350 次,将实验电池放电至3.0 V,即SOC=0%,拆解电池后取极片烘干,用刀片刮取极片上涂敷的活性物质,混入10%~20%的硅粉,然后研磨成无结块、混料均匀的粉体。混料前,硅粉须进行真空退火热处理,热处理时间1 h,温度为1 100 ℃。利用岛津6100型X 射线衍射仪分析粉体的物相,正极活性物质扫描范围18°~29°,扫描速度0.1 (°)/min,负极活性物质扫描范围25°~29°,扫描速度0.1 (°)/min。利用JADE 6.0 软件计算锰酸锂(111)晶面间距d(111)与石墨(002)晶面间距d(002)。晶面间距变化率采用式(2)计算:

式中:di(klh)为电池循环i次后实测晶面间距;
d(klh)为理论晶面间距;
d(111)取0.476 38 nm;
d(002)取0.337 56 nm。
1.4 ICP 测试
将极片上涂覆的活性物质称重后置于烧杯中,加入足量的硝酸,煮沸3 min 后,过滤后取10 mL 滤液放入250 mL 的容量瓶中,加蒸馏水至液面到达容量瓶250 mL 刻度线,选用1×10-6、2×10-6、4×10-6、8×10-6μg/mL 的Li、Mn 标准溶液。利用iCap 6000 型电感耦合等离子体发射光谱仪测量粉体内Li、Mn 元素质量分数。
2.1 不同阶段的充放电性能
图2 为实验电池与三电极电池高温循环测试曲线。由图可看出,随着循环次数的增加,实验电池容量保持率逐渐降低,且三电极电池与实验电池容量保持率基本保持同步衰减,即软包电池中塞入锂参比电极不影响电池充放电测试。前50 次循环容量减少较快,而后减少速率变慢,且减少速率近似恒定,循环至350 次,电池容量损失23%。

图2 电池容量保持率-循环曲线
2.2 正负极片电极电位
图3 为三电极电池不同循环次数的电极电位曲线。图3(a)为不同循环次数充电过程中正极电位曲线,首次充电时,随充电时间的延长,正极电位逐渐正移,当电极电位正移至4.04 V 时,正移速度变缓,出现一个电压平台,该过程代表LiMn2O4向LixMn2O4转变的单相化学反应,其中x取0.6~0.7[18-19];
当充电至4 800 s 左右时,电极电位正移速度加快,而后上升至4.12 V,正移速度再次变缓,出现第二个电位平台,该过程代表LixMn2O4向λ-MnO2转变的单相化学反应[18-19],最后电极电位急剧正移至4.33 V,恒流充电结束。随着循环的进行,正极电位曲线整体正移,4.04、4.12 V 的电位平台逐渐变短,且4.12 V 电压平台变短、消失速度快于4.04 V 电压平台。图3(b)为不同循环次数充电过程中负极电位曲线,在循环测试过程中,负极电位曲线,近似呈一条水平的直线,即未能显示由石墨嵌锂引起的电极电位的起伏,这是由于嵌锂引起的电位起伏低于数据记录仪的精度,随着循环测试的进行,水平的直线正移,且变短。图3(c)为不同循环次数放电过程中正极电位曲线,其变化与图3(a)所呈现的变化趋势相反,其首次放电电位平台分别在4.09、3.96 V。图3(d)为不同循环次数放电过程中负极电位曲线,在循环测试过程中,负极电位曲线仍近似呈一条水平的直线,且无起伏,随着循环测试的进行,水平的直线负移、变短。比较图3(a)和(b)可看出,随循环次数的增加,正极电位曲线正移的幅度明显大于负极电位曲线负移的幅度;
比较图3(c)和(d)可看出,随循环次数的增加,正极电位曲线负移的幅度明显大于负极电位曲线正移的幅度。

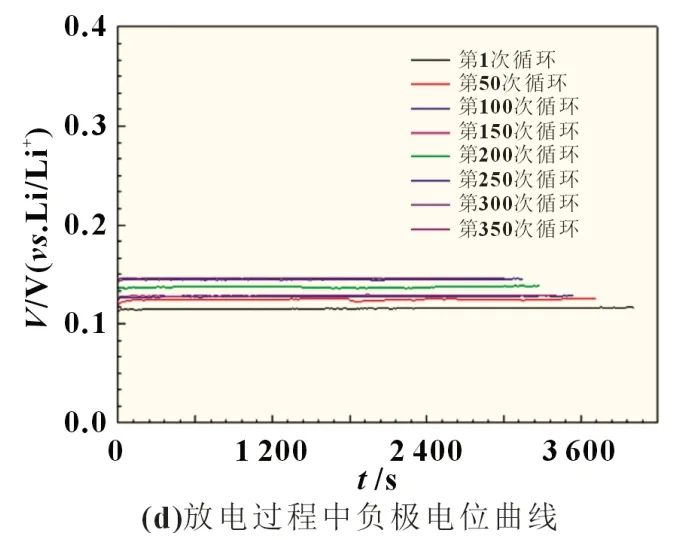
图3 不同循环次数正负极电极电位曲线
2.3 活性物质ICP 检测结果
图4 为不同循环次数正负极活性物质ICP 检测结果。由图4(a)可看出,循环一次后,正极活性物质中Li 元素质量分数为3.54%,锰酸锂中Li 元素的理论质量分数为5.07%,这种差异是由于SEI 膜形成过程中消耗了部分活性锂和活性物质中添加的导电剂、粘结剂。随着循环的进行,正极活性物质中Li 元素质量分数缓慢降低,循环至350 次,降低至3.26%;
循环一次后,负极活性物质中Li 元素质量分数为0.87%,其主要原因是石墨表面的SEI 膜与石墨中未脱嵌的Li 造成的[19-21];
随循环次数的增加,Li 元素质量分数逐渐上升,这是由于SEI膜的生长[19-21]。由图4(b)可看出,初次循环后,负极活性物质中Mn 元素质量分数为0.09%,循环至50 次,急剧增至0.16%,而后缓慢增加。


图4 ICP测试结果
2.4 活性物质XRD 分析
图5 为正负极活性物质的X 射线衍射图谱。图5(a)为正极活性物+硅粉的X 射线衍射图谱,其中2 θ=18.6°峰代表锰酸锂(111)晶面的衍射峰,2 θ=28.4°峰代表硅粉(111)晶面的衍射峰,消除仪器误差后得到不同循环次数锰酸锂(111)晶面的衍射峰位置分别在18.689°(第1 次循环)、18.692°(第50 次循环)、18.699°(第100 次循环)、18.705°(第150 次循环)、18.711°(第200 次循环)、18.735°(第250 次循环)、18.765°(第300 次循环)、18.765°(第350 次循环)。图5(b)为负极活性物+硅粉的X射线衍射图谱,其中2 θ=26.4°峰代表石墨(002)晶面的衍射峰,2 θ=28.4°峰代表硅粉(111)晶面的衍射峰,消除仪器误差后得到不同循环次数石墨(002)晶面的衍射峰,位置分别在26.497°(第1 次循环)、26.494°(第50 次循环)、26.506°(第100 次循 环)、26.508°(第150次循环)、26.500°(第200次循环)、26.504°(第250 次循环)、26.497°(第300次循环)、26.513°(第350 次循环)。图5 (c)为不同循环次数锰酸锂(111)、石墨(002)晶面间距的变化率,其中晶面间距由布拉格方程2dsin θ=nλ算出。由图可知,首次循环后,锰酸锂(111)、石墨(002)晶面间距的变化率分别为-5.540%、0.449%,其中变化率为正值表示晶面间距变大,变化率为负值表示晶面间距变小,这是由于锰酸锂中部分Li 元素被消耗、石墨中部分Li 元素未脱嵌。随着循环次数的增加,锰酸锂(111)晶面间距变化率逐渐变小,石墨(002)晶面间距基本维持恒定,这说明随循环的进行,锰酸锂晶格逐步收缩,石墨晶格基本无变化。

图5 活性物质X射线衍射结果
本文研究了12 Ah 锰酸锂-石墨锂离子电池高温循环测试过程中容量减少的问题,由图2 可看出,循环测试至100 次时电池容量损失了10.60%,容量保持率的平均衰减速率0.106%/次;
100~350 次循环测试过程中,电池容量衰减速度略减缓,且容量衰减速率基本恒定,电池容量衰减了12.10%,期间容量保持率的衰减速率为0.048%/次。锰酸锂高温循环容量减少的可能原因有:Mn 溶解、Jahn-Teller 效应、锰酸锂晶体缺陷与高温下两相结构稳定性的降低。负极石墨容量减少的原因为SEI 膜的生长,SEI 膜由LiF、烷基锂、Li2CO3等物质组成[19-21]。由图4 可知,前100 次循环测试后,SOC=0%状态下负极Li、Mn 元素含量增量均较大,一方面,负极Li 元素的含量升高表明在循环初期SEI 膜的生成与生长,其生成与生长均会消耗活性锂源;
另一方面,循环前期(1~100 次)负极Mn 元素的含量急剧增大表明锰的溶解。Xia 等[22]研究了锰酸锂在30 与50 ℃循环50 次后锰酸锂容量的损失,结果表明,Mn 元素的溶解分别造成了23%和34%的容量损失。由X 射线衍射结果(图5)可知,前100 次循环测试过程中,正负极活性物质结构无明显变化,因而可认为前100 次循环测试,电池容量衰减的原因为:Mn 元素的溶解、SEI 膜的生成与生长。
循环至100~350 次时,电池容量衰减速率变缓,负极活性物质中Li、Mn 元素的含量缓慢增加,增幅速率明显小于前100 次循环测试,而且LiMn2O4(111)晶面间距明显变小,说明锰酸锂的晶体结构发生了变化。负极活性物质Li 元素的缓慢增加表明SEI 膜的生长。目前,普遍认为LiMn2O4在3 V 区域进行充放电时会出现Jahn-Teller 畸变,Jahn-Teller 畸变会导致锰酸锂的结构变化,进而导致锰酸锂容量减少,关于Jahn-Teller 畸变的机理,目前还有争议。由图5 可看出,Jahn-Teller畸变引起的结构变化与Mn 溶解引起的结构变化(0~50 次)有着本质区别。Mn 元素溶解会产生一些低电化学活性或无电化学活性的物质,如Li2MnO3,Li2Mn4O9等[23],而Jahn-Teller 畸变会引起Mn3+O6八面体畸变或立方相转变为正交相[24-26]。因而可认为,100~350 次循环测试过程中电池容量减少的原因有:Jahn-Teller 畸变引起的锰酸锂晶体结构变化、Mn 元素溶解与SEI 膜的生长。
由图3 可看出,随循环测试的进行,充电过程中正极电位曲线整体逐渐正移,负极电位曲线整体逐渐负移,放电过程中正极电位曲线逐渐负移,负极电位曲线逐渐正移,即正负极极化逐渐变大。Robertson 的研究[23]指出,Mn 溶解的产物Li2MnO3和Li2Mn4O9会堵塞Li+的扩散通道。Wang 等[7]研究了尖晶石结构正极材料容量衰减机制,验证了氧缺陷会通过某种方式破坏Li+的三维扩散通道。可推测如锰酸锂(111)晶面收缩引起的晶体结构变化也会妨碍Li+的固相扩散过程。因而,正极极化的增加可归咎于Mn 溶解的副产物堵塞Li+的扩散通道与晶格收缩妨碍了Li+的固相扩散过程。Amine 等[11]认为溶解的Mn 元素以Mn 单质的形式沉积在负极上,沉积在负极的Mn 会增大石墨脱嵌锂的阻力。因而,负极极化增大的原因是Mn 的沉积与SEI 膜的生长。
(1) 高温循环测试过程中,锰酸锂-石墨电池容量减少的原因是Mn 的溶解、锰酸锂晶体结构的变化和SEI 的生成与生长。
(2)循环测试过程中正极极化增加的原因是:锰酸锂晶体结构的变化与Mn 溶解的副产物堵塞Li+扩散通道,负极极化增加的原因是:SEI 膜的生长与Mn 的沉积。
猜你喜欢 晶面电池容量负极 脉状负极石墨性能优于领先的商业合成石墨汽车工程师(2021年12期)2022-01-18MXene@Sn4P3复合材料的制备及在锂离子电池负极材料中的应用研究陶瓷学报(2020年3期)2020-10-27对接充电系统电动工具(2020年2期)2020-04-22NaCl单晶非切割面晶面的X射线衍射物理实验(2019年7期)2019-08-06恒流电池容量测试仪的设计智富时代(2019年6期)2019-07-24恒流电池容量测试仪的设计智富时代(2019年6期)2019-07-24(100)/(111)面金刚石膜抗氧等离子刻蚀能力航空材料学报(2019年2期)2019-04-15立方晶格晶面间距的计算云南民族大学学报(自然科学版)(2015年4期)2015-11-14一种单晶光学晶体的晶面偏角及偏向测算方法中国新技术新产品(2014年4期)2014-03-12超细化/复合化锡基负极纳米材料在锂离子电池上的研究进展储能科学与技术(2014年5期)2014-02-27